PhytoLab, l’un des principaux fabricants dans le monde, propose plus de 1 500 substances végétales de référence, largement documentées, de toutes les classes de composés naturels. Notre gamme comprend actuellement un total de 28 glucosinolates ainsi que le produit de dégradation goitrogène DL-goitrine. La plupart de nos glucosinolates et composés apparentés sont certifiés en tant qu’étalons de référence primaires.

Glucosinolates
Présence et propriétés
Les glucosinolates sont des métabolites végétaux secondaires présents dans une grande variété de plantes appartenant principalement aux familles des Brassicaceae (par ex. raifort (Armoracia rusticana), radis (Raphanus sativus), wasabi (Eutrema japonicum), moutarde noire (Brassica nigra), moutarde blanche (Sinapis alba), brocoli (Brassica oleracea var. italica), colza (Brassica napus), maca (Lepidium meyenii), crambe (Crambe abyssinica), alysson argenté (Alyssum argenteum), cameline (Camelina sativa), cresson d'hiver (Barbarea vulgaris), cresson de fontaine (Nasturtium officinale), alysson blanc (Berteroa incana), giroflée des murailles (Cheiranthus cheiri), roquette (Eruca sativa), Julienne des dames (Hesperis matronalis), ibéris amer (Iberis amara) et pastel des teinturiers (Isatis tinctoria)), les Capparaceae (par ex. câprier commun (Capparis spinosa)) et les Caricaceae (par ex. papayer (Carica papaya)), mais aussi les Euphorbiaceae, les Tropaeolaceae (par ex. capucine des jardins (Tropaeolum majus)), les Cleomaceae (par ex. fleur d’araignée épineuse (Cleome spinosa)), les Limnanthaceae (par ex. limnanthe de Douglas (Limnanthes douglasii)) et les Moringaceae (par ex. moringa (Moringa oleifera)).
Outre le fait qu’ils sont responsables du goût piquant et amer de ces plantes, les glucosinolates et leurs produits d’hydrolyse protègent également les plantes des herbivores et possèdent des propriétés antimicrobiennes, antivirales, antifongiques et anticancérigènes. En raison de leurs propriétés antimicrobiennes, les produits médicinaux à base de plantes contenant de la capucine herbacée et de la racine de raifort sont utilisés dans le traitement de la sinusite, de la bronchite et des infections des voies urinaires. La Commission E allemande a publié une monographie sur le raifort (Armoraciae rusticanae radix) en 1988.
Structure des glucosinolates et des composés dérivés

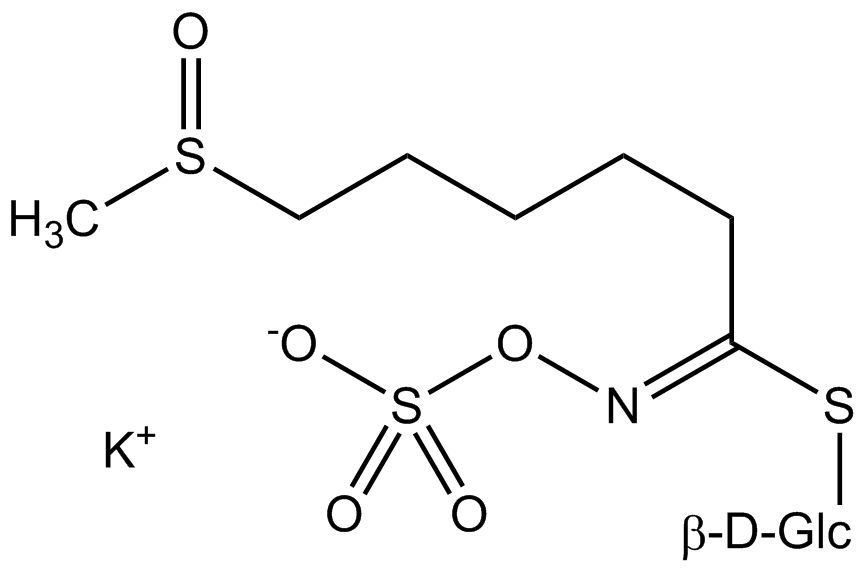
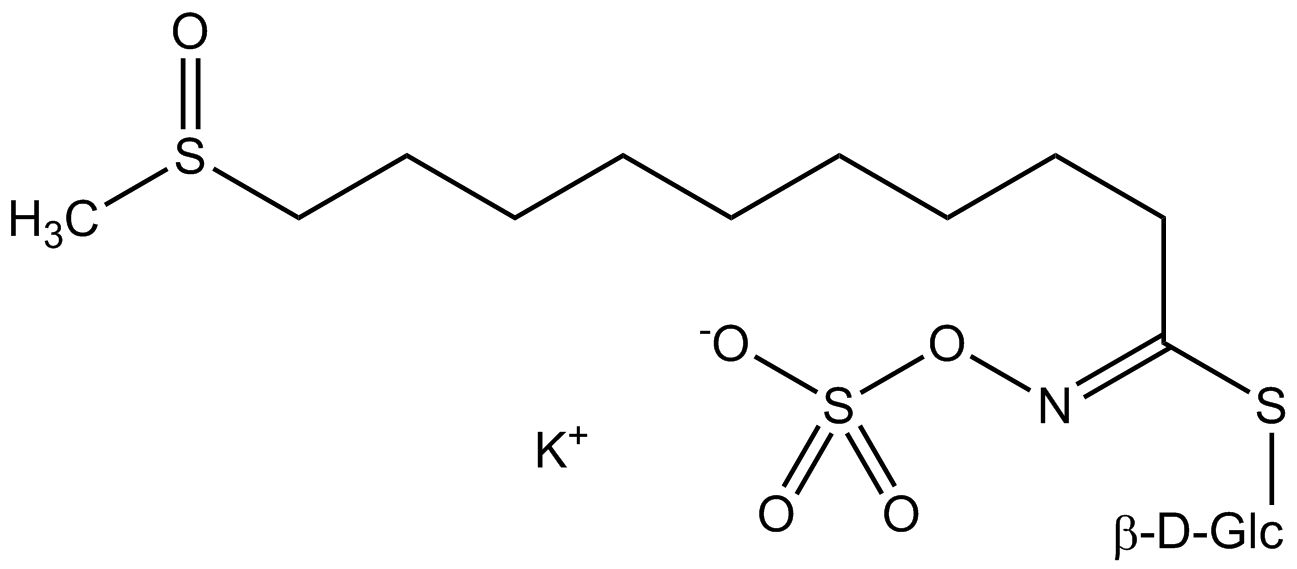
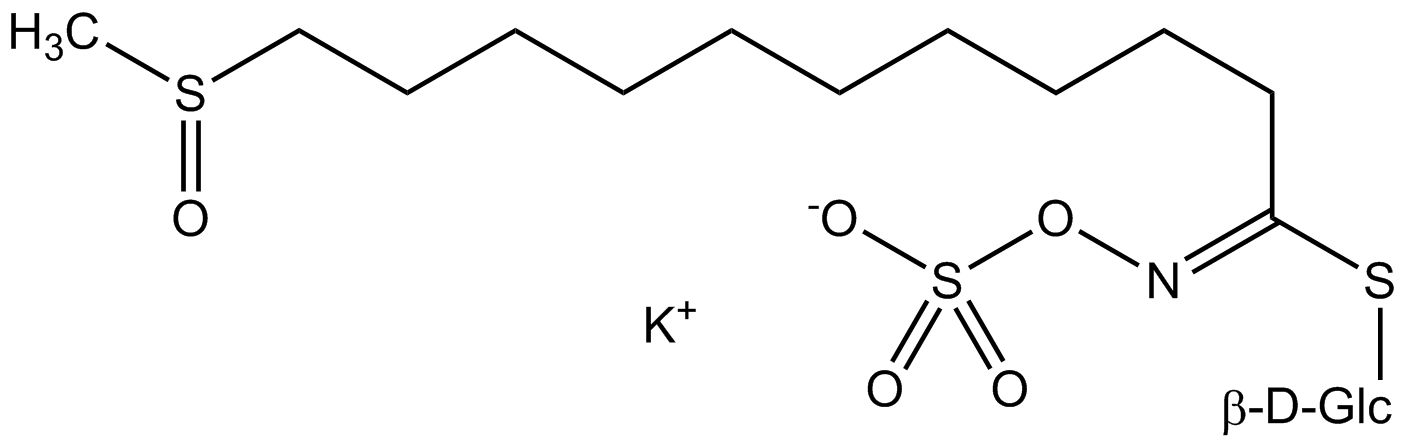
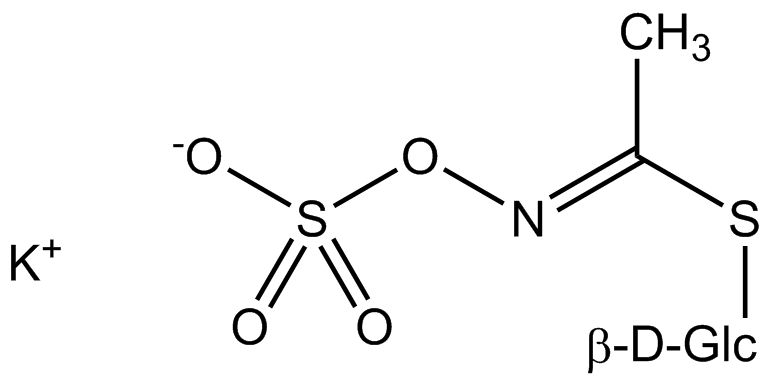
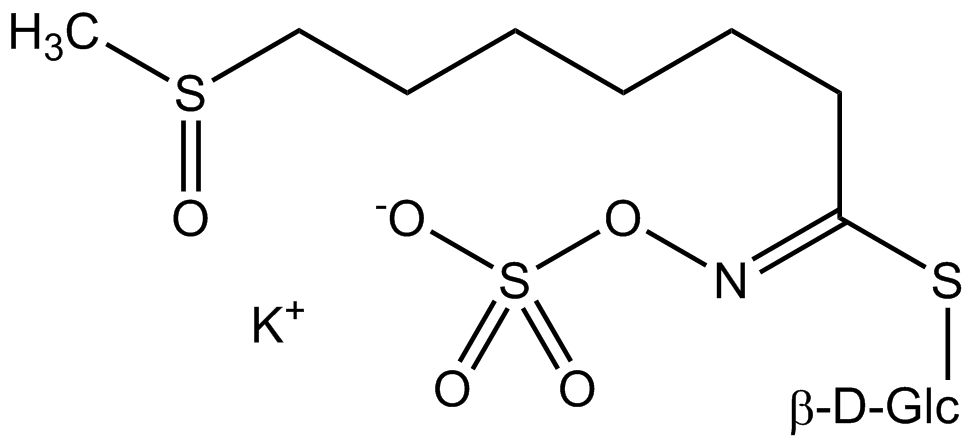
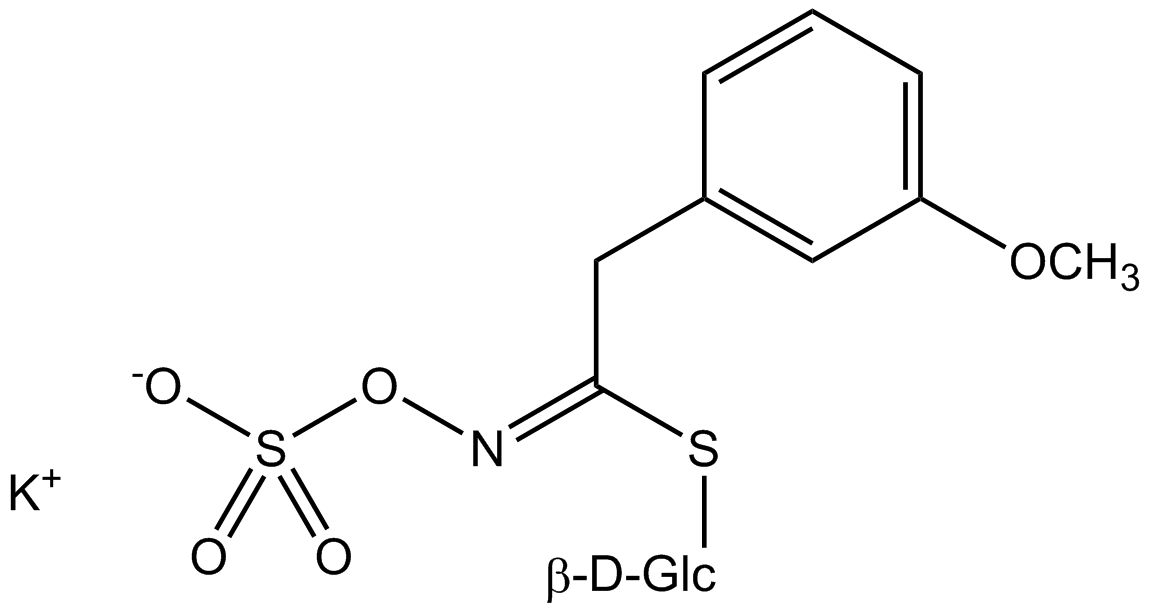
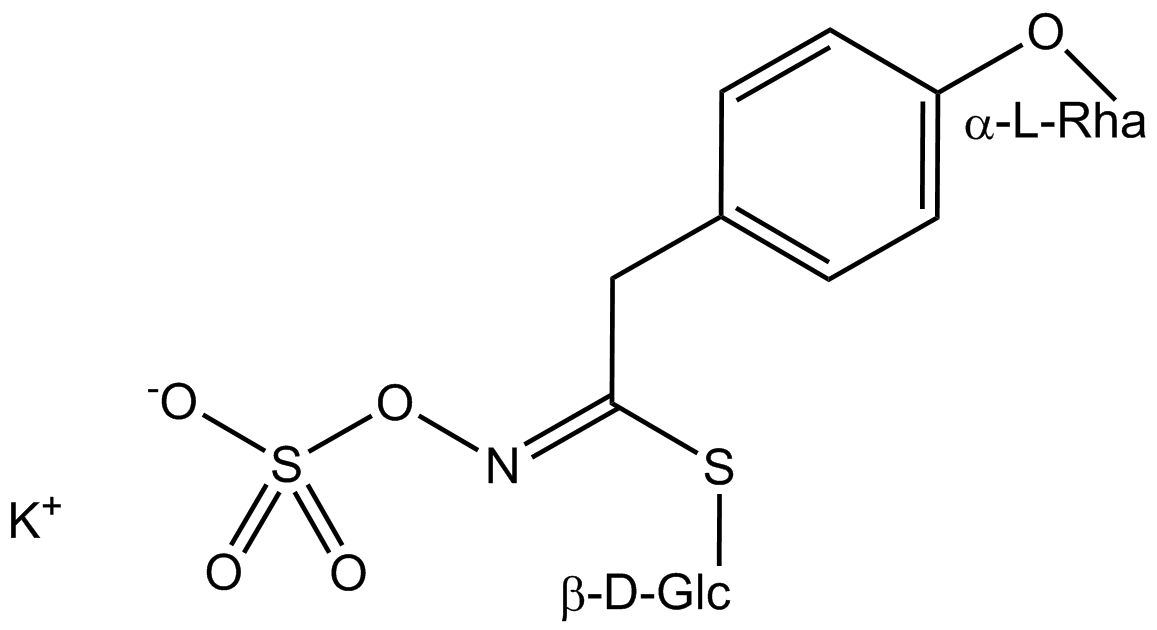
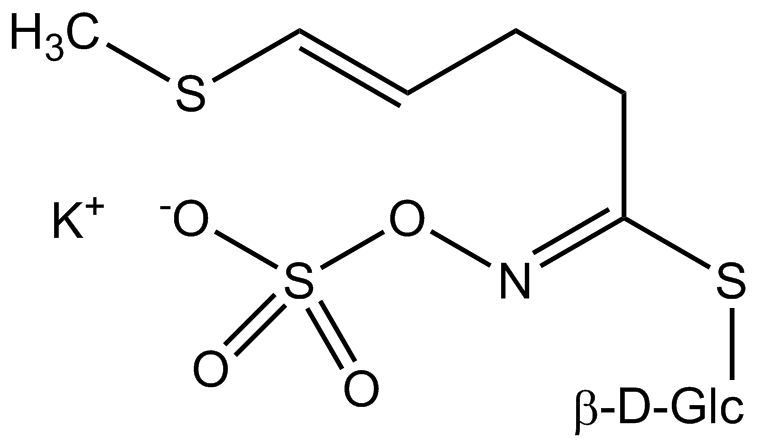
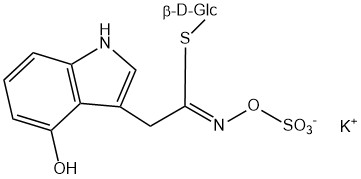
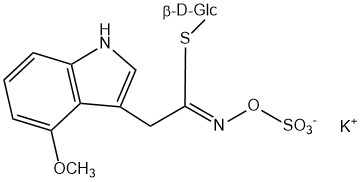
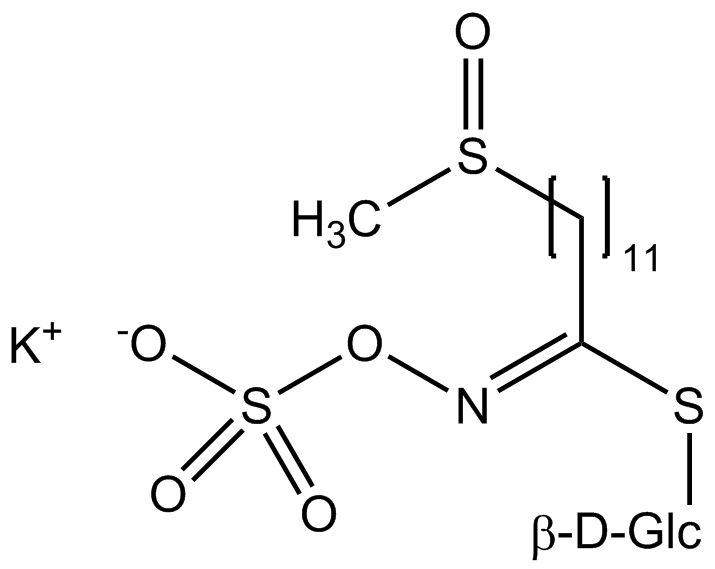
Tous les glucosinolates sont composés d’un carbone central lié par un atome de soufre à un glucose et par un atome d’azote à un groupe sulfate. En outre, une chaîne latérale spécifique à la substance (dont la structure dépend de l’acide aminé impliqué dans la phase initiale de la biosynthèse du glucosinolate) est liée à l’atome de carbone central. Le groupe sulfate étant chargé négativement, les glucosinolates sont le plus souvent isolés sous la forme de leurs sels de potassium. La biosynthèse des glucosinolates qui portent une chaîne latérale alkyle ou soufrée (comme les groupes thiométhyl-, sulfinyl- ou sulfonyl) commence le plus souvent à partir des groupes suivants methionine (comme epiprogoitrine, glucoalyssine, glucoarabine, glucoberteroïne, glucobrassicanapine, glucocamélinine, glucocapparine, glucocheiroline, glucoérucine, glucohespérine, glucoibérine, gluconapine, glucoraphanine, glucoraphasatine, glucoraphénine, 11-méthylsulfinylundécylglucosinolate, progoitrine et sinigrine). La biosynthèse des glucosinolates ayant un anneau phényle ou benzyle dans la structure centrale commence à partir de la phénylalanine ou de la tyrosine (par ex. glucobarbarine, glucolimnanthine, glucomoringine, gluconasturtiine, glucotropéoline et sinalbine), tandis que les chaînes latérales contenant de l’indolyle, comme dans la glucobrassicine, 4-Hydroxyglucobrassicine, 4-Methoxyglucobrassicine et Neoglucobrassicine proviennent de l’acide aminé tryptophane.
Au contact de l’enzyme myrosinase et de l’eau (la myrosinase est conservée dans un compartiment séparé de la cellule, mais peut être libérée, par exemple, lors de la coupe ou de la mastication), la partie glucose est clivée. La molécule restante peut alors subir diverses réactions spontanées, qui aboutissent généralement à l’isothiocyanate correspondant. En fonction des conditions de réaction, des thiocyanates, des nitriles ou des oxazolidines 2-thiones tels que la goitrine peuvent également être formés.

Glucosinolates : structure de la chaîne latérale et isothiocyanates dérivés
| Glucosinolate | Chaîne latérale R | Isothiocyanate correspondant |
|---|---|---|
| Épiprogoitrine | CH2=CH–CHOH–CH2– | 2(S)-hydroxy 3-butenylisothiocyanate |
| Glucoalyssine | CH3–SO–(CH2)5- | 5-(méthylsulfinyl)pentylisothiocyanate |
| Glucoarabine | CH3–SO–(CH2)9- | 9-(méthylsulfinyl)nonylisothiocyanate |
| Glucobarbarine | C6H5–CHOH–CH2– | 2(S)-Hydroxy 2-phényléthylisothiocyanate |
| Glucoberteroïne | CH3–S–(CH2)5– | 5-(méthylthio)pentylisothiocyanate |
| Glucobrassicanapine | CH2=CH2–(CH2)3– | 4-pentenylisothiocyanate |
| Glucobrassicine | 3-indolylméthyl- | 3-indolylméthylisothiocyanate |
| Glucocamélinine | CH3–SO–(CH2)10- | 10-(méthylsulfinyl)décylisothiocyanate |
| Glucocapparine | CH3– | méthylisothiocyanate |
| Glucocheiroline | CH3–SO2–(CH2)3– | 3-(méthylsulfonyl)propylisothiocyanate |
| Glucoérucine | CH3–S–(CH2)4– | 4-(méthylthio)butylisothiocyanate |
| Glucohespérine | CH3–SO–(CH2)6- | 6-(méthylsulfinyl)hexylisothiocyanate |
| Glucoibérine | CH3–SO–(CH2)3– | 3-(méthylsulfinyl)propylisothiocyanate |
| Glucolimnanthine | OCH3-C6H5–CH2– | 3-méthoxybenzylisothiocyanate |
| Glucomoringine | 4-O-Rhamnosy-C6H4–CH2– | 4-(rhamnosyloxy)benzylisothiocyanate |
| Gluconapine | CH=CH–(CH2)2– | 3-butenylisothiocyanate |
| Gluconasturtiine | C6H5–(CH2)2– | 2-phényléthylisothiocyanate |
| Glucoraphanine | CH3–SO–(CH2)4– | sulforaphane |
| Glucoraphasatine | CH3–S–CH=CH–(CH2)2– | 4-(méthylthio)-3-buténylisothiocyanate |
| Glucoraphénine | CH3–SO–CH=CH–(CH2)2– | sulforaphène |
| Glucotropéoline | C6H5–CH2– | benzylisothiocyanate |
| 4-Hydroxyglucobrassicine | 4-Hydroxy-3-indolylméthyle | 4-Hydroxy-3-indolylméthylisothiocyanate |
| 4-Methoxyglucobrassicine | 4-Méthoxy-3-indolylméthyle | 4-Méthoxy-3-indolylméthylisothiocyanate |
| 11-méthylsulfinylundécyl-glucosinolate | CH3–SO–(CH2)11- | 11-(méthylsulfinyl)undécylisothiocyanate |
| Neoglucobrassicine | N-Méthoxy-3-indolylméthyle | N-Méthoxy-3-indolylméthylisothiocyanate |
| Progoitrine | CH2=CH–CHOH–CH2– | 2(R)-hydroxy-3-butenylisothiocyanate |
| Sinalbine | 4-OH-C6H4–CH2– | 4-hydroxybenzylisothiocyanate |
| Sinigrine | CH2=CH–CH2– | allylisothiocyanate |
Recommandation
Pour une analyse quantitative fiable des glucosinolates et de leurs produits de dégradation, il est essentiel de disposer de substances de référence bien caractérisées. Nous proposons actuellement 28 glucosinolates ainsi que le produit de dégradation goitrogène DL-goitrine, tous fournis avec un certificat d’analyse complet. En raison de la charge négative de la structure centrale du glucosinolate, le contre-ion doit être pris en compte. Pour tous les glucosinolates caractérisés comme étalon de référence primaire, le potassium a été déterminé quantitativement et considéré comme une impureté dans le calcul de la teneur absolue, qui se réfère donc uniquement au glucosinolate pur.
Pour obtenir des informations actualisées sur les prix et les spécifications, veuillez consulter les pages détaillées des produits ci-après !